반응형
카페인 표준품 성적서 해석

1. 기본 정보
- 제품명: Caffeine (카페인)
- 제품번호: PHR1009-1G
- 로트 번호: LRAD7001
- 유효기간: 2028년 3월 31일까지
- 보관 조건: 2–30°C, 빛 차단 필요
- 형태: 백색 분말
- 화학식: C₈H₁₀N₄O₂
- 분자량: 194.2
- CAS 번호: 58-08-2
2. 인증 순도 (Certified Purity)
- 순도: 99.97%
- 불확도: ± 0.11% (확장 불확도, k=2)
- 기준: 질량평형법(Mass Balance, As-is 기준)
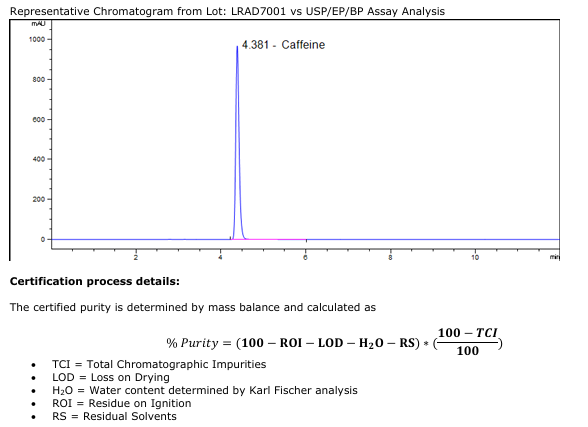
Mass Balance = 100 - (총 크로마토그래피 불순물 + 건조 손실 + 수분 + 점화 잔류물 + 잔류 용매)
3. 분석 및 시험 방법
HPLC 분석법
- 컬럼: Ascentis Express C18, 150mm x 4.6mm, 5µm
- 이동상: 아세트산나트륨(pH 4.5), 아세토니트릴, 테트라하이드로푸란 혼합
- 유속: 1.0 mL/min
- 검출기: DAD, 파장 275 nm
NMR 및 IR, MS, 녹는점
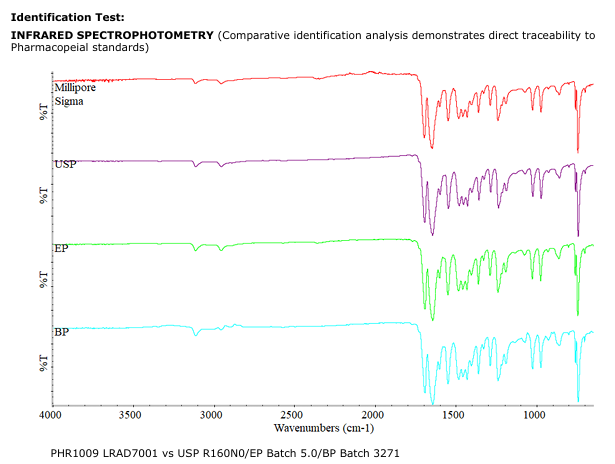
- IR 분석: USP/EP/BP 표준과 비교해 구조 일치 확인
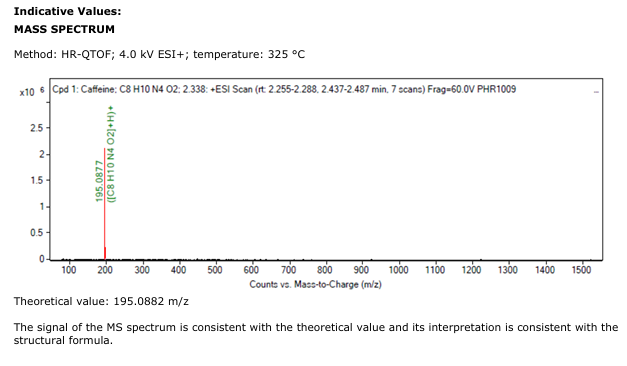
- 질량 분석 (MS): 195.0882 m/z (이론값과 일치)
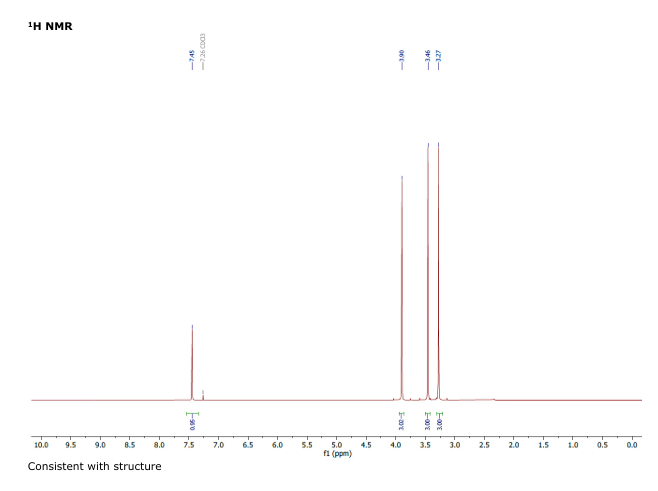
- ¹H NMR: 구조와 일치
- 녹는점: 평균 237.3°C (EP 기준 234–239°C 범위 내)
4. 불순물 및 안정성 정보
- 총 불순물: 0.026% (HPLC로 검출)
- 잔류용매: 없음 (GC-MS 확인)
- 건조손실 / 회분 잔류물: 없음
- 동질성 평가: 통계적으로 동질성이 입증됨 (ANOVA 분석)
- 단기 및 장기 안정성 평가 수행됨
5. 추적성 및 인증
- SI 단위 및 NIST 표준에 따라 추적성 보장
- ISO 17034 인증 (AR-1470) 및 ISO 17025 교정된 저울 사용
- USP, EP, BP 기준물질과 비교분석함
결론 및 활용 시 주의사항
- 연구용 또는 시험 분석용 이외의 용도(예: 약물 제조, 가정용 등)로 사용할 수 없습니다.
- 최소 샘플 사용량은 10 mg이며, 별도 건조 없이 '있는 그대로(as-is)' 사용해야 합니다.
- 보관 중 압력 차이로 개봉 시 분산 위험이 있으니 주의해야 합니다.
- 미사용 분량은 20mm 알루미늄 실로 밀봉 권장


📌 "순도: 99.97%"
→ 이 카페인 표준물질(CRM)은 전체 질량 중 99.97%가 순수한 카페인이라는 뜻입니다. 나머지 0.03%는 불순물, 수분, 잔류 용매 등일 수 있습니다.
📌 "불확도: ± 0.11%"
→ 이 수치는 측정값의 오차 범위를 의미합니다.
즉, 실제 순도는 99.97% ± 0.11%,
즉 99.86% ~ 100.08% 사이일 가능성이 95% 있다는 뜻입니다.
📌 "(확장 불확도, k=2)"
→ 이건 통계적으로 신뢰도를 말하는 지표입니다.
- k=2는 **신뢰도 95%**를 의미합니다.
- "확장 불확도(Expanded Uncertainty)"란 표준불확도(standard uncertainty)를 2배 해서 보다 넓은 신뢰구간을 잡은 것입니다.
반응형
'품질관리(Quality Control) > 제약' 카테고리의 다른 글
| 10년 이상 현직 제약회사 QC 실무자가 쓴 실무 기반 블로그 (16) | 2025.07.04 |
|---|---|
| 제약회사 품질관리 취업 준비자의 성격과 적성 파악 (20) | 2025.06.20 |
| 제약회사 품질관리 QC 취업하려면? 꼭 필요한? 스펙 및 하는일 알려줄게 (59) | 2025.06.10 |
| 제약회사 품질관리 엑셀 계산 정확하게 사용하는 방법 (10) | 2025.06.05 |
| 테일링 계수 Tailing factor, 대칭 계수 Symmetry factor 같은 것인가요? (종결) (4) | 2025.05.27 |
